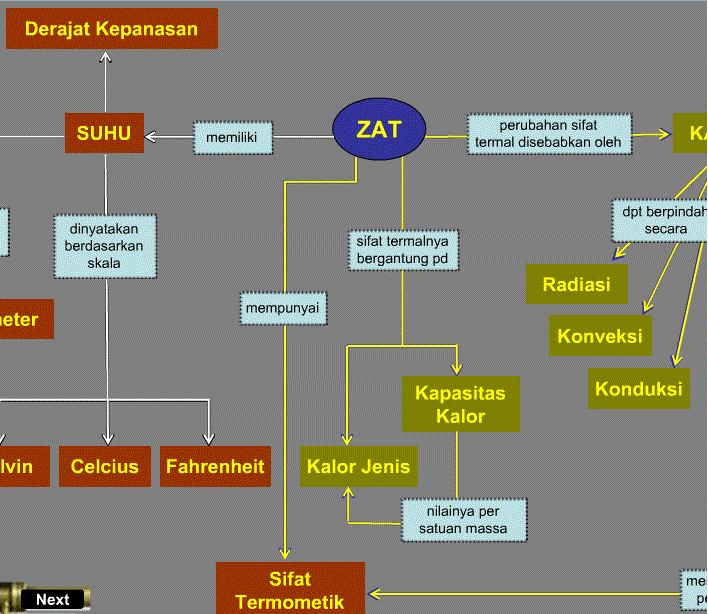
Pada bagian berikut akan dibahas terkait konsep perubahan wujud zat. Pembahasan diawali dengan meninjau pengertian kalor. Kalor merupakan energi yang berpindah, artinya begitu proses pemindahan energi berhenti, maka kalor tidak memiliki arti lagi. Jika suatu zat diberikan kalor, maka kemungkinan peristiwa yang terjadi pada zat tersebut antara lain:
1. Zat tersebut akan mengalami kenaikan suhu seperti ketika memanaskan air/logam.
2. Zat tersebut tidak mengalami perubahan suhu seperti ketika memanaskan es hingga es mencair, pada saat mencair es tersebut mengalami perubahan wujud dari padat menjadi cair. Jadi kalor yang diberikan digunakan untuk mengubah wujudnya bukan untuk menaikkan suhunya sehingga suhunya tetap.
3. Zat tersebut dapat mengalami perubahan wujud misalnya menjadi cair atau gas.
4. Massa jenis benda akan berkurang sebab ketika dipanaskan benda akan memuai, akibatnya volume benda bertambah sedangkan massanya tetap.
Sekarang kita akan membahas pengaruh kalor dalam mengubah wujud zat. Ada enam perubahan wujud zat yang dikenal yaitu mencair, menguap dan menyublim memerlukan kalor sedangkan membeku, mengembun, dan deposisi melepaskan kalor. Perhatikan Gambar 1.4.1 menunjukkan tentang diagram perubahan wujud zat.
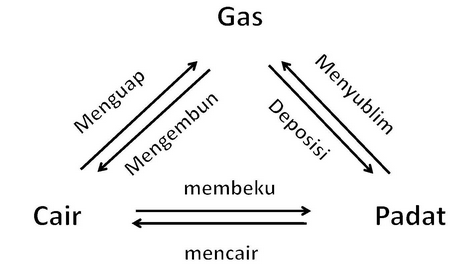
Gambar 1.4.1 Diagram perubahan wujud zat
Jika es dipanaskan, maka dalam beberapa waktu es akan berubah wujud menjadi air, selanjutnya air akan berubah menjadi uap bila pemanasan terus dilakukan. Demikian pula jika uap didinginkan, beberapa waktu kemudian uap air akan berubah menjadi air dan bila air didinginkan akan berubah menjadi es. Berikut disajikan contoh diagram pemanasan es hingga menjadi uap pada tekanan 1 atm.
Gambar 1.4.2. Grafik pemanasan es hingga menjadi uap
Pada saat mengalami perubahan wujud, kalor yang diberikan digunakan untuk mengubah wujud zat bukannya untuk menaikkan suhunya sehingga pada fase perubahan wujud seperti mencair (ditunjukkan oleh garis BC pada Gambar 1.4.2), menguap (ditunjukkan oleh garis DE pada Gambar 1.4.2) dan lainnya suhu zat akan tetap. Pada diagram biasanya ditunjukkan dengan tanda garis mendatar yang menandakan suhu zat tetap.
Berdasarkan grafik Gambar 1.4.2 tersebut terdapat proses perubahan temperatur dan wujud zat yang terjadi, yakni sebagai berikut.
a. Proses A – B merupakan proses kenaikan temperatur dari sebongkah es. Pada proses kenaikan temperatur ini, grafik yang terjadi adalah linear. Pada grafik AB, kalor digunakan untuk menaikkan temperatur.
QAB = mes cesΔT
QAB = mes ces (0oC – (–T1))
QAB = mes ces T1 (1.3.1)
b. Proses B – C merupakan proses perubahan wujud zat dari es menjadi air. Pada grafik BC, kalor tidak digunakan untuk menaikkan atau menurunkan temperatur benda, tetapi hanya digunakan untuk mengubah wujud zat benda tersebut, yakni dari wujud es menjadi air.
QBC = mesL (1.3.2)
c. Pada grafik C – D, terjadi proses kenaikan temperatur yang sama dengan proses pada (a). Akan tetapi, pada proses ini yang dinaikkan suhunya adalah air dari 0oC sampai 100oC.
QCD = maircair ΔT
QCD = maircair (100°C – 0°C)
QCD = maircair 100°C (1.3.3)
d. Sama halnya pada proses B – C, proses D – E tidak mengalami perubahan temperatur, tetapi yang terjadi hanya perubahan wujud zat dari air menjadi uap.
QDE = mairL (1.3.4)
Zat dapat berwujud padat, cair, atau gas. Ketiga macam wujud zat itu fase padat, fase cair, dan fase gas. Fase padat dari air (H20) adalah es, fase cairnya adalah air, dan fase uapnya adalah uap air. Semua zat dapat berwujud padat, cair dan gas, asal zat itu tidak terurai atau terdekomposisi pada temperatur tinggi.
Peralihan atau transisi dari fase yang satu ke fase yang lain disertai penyerapan atau pengeluaran kalor .
Contoh 1.4.1
Berikanlah argumentasi mengapa dinding luar gelas yang berisi es timbul titik-titik air seperti pada Gambar 1.4.3 di bawah?

Gambar 1.4.3.Butir-butiran air
pada dinding gelas yang beiri es
Penyelesaian:
Bintik-bintik air tersebut sebenarnya berasal dari peristiwa pengembunan udara yang berada di sekitar dinding gelas. Udara mengalami pengembunan karena udara di sekeliling gelas melepaskan kalor kepada es dalam gelas sebab suhu udara lebih besar daripada suhu es dalam gelas. Karena udara melepaskan kalor makanya udara berubah wujud menjadi air, yang kita lihat berupa titik-titik air di luar gelas.
Contoh 1.4.2: Pemecahan masalah
Sebuah lemari es bermerek Sharp dibeli oleh Ade. Ia ingin membuka usaha pembuatan es lilin karena telah di PHK dari kantor tempat ia bekerja. Ia ingin es lilin yang dibuatnya dengan massa 10 gram tidak cepat mencair yakni dengan suhu -150C. Jika suhu awal air bahan es lilin tersebut adalah 200C, cobalah evaluasi kalor yang harus dikeluarkan lemari es tersebut agar es lilin yang dihasilkan sesuai dengan keinginan Ade! Kalor lebur es 334 ×103 J/kg, kalor jenis es 2100 J/kg 0C, kalor jenis air 4186 J/kg 0C.
Penyelesaian:
Visualisasi masalah: Variabel-variabel yang teridentifikasi:menunjukkan bukti pemahaman konsep
Diketahui:
Massa air = massa es lilin = 10 gram = 0,01 kg
Suhu akhir, Takhir = -150C
Suhu awal, Tawal = 200C
cair = 4186 J/kg C0
ces = 2100 J/kg C0
Lf = 334 ×103 J/kg
Ditanyakan:
Rancanglah kalor yang harus dikeluarkan oleh lemari es (Qtotal)? (Joule)
Deskripsi Fisika
Kesesuaian persamaan dengan deskripsi
- Menentukan kalor yang dilepas air 200C untuk menjadi air 00C dengan persamaan
- Menentukan kalor yang dilepas air 00C untuk membeku seluruhnya menjadi es 00C dengan persamaan
- Menentukan kalor yang dilepas es 00C untuk menjadi es -150C dengan persamaan
- Menentukan total kalor yang dilepas dengan persamaan
Rencana solusi yang masuk akal
- Kalor yang dilepas air 200C untuk menjadi air 0 0C:
- Kalor yang dilepas air 00C untuk membeku seluruhnya menjadi es 00C
- Kalor yang dilepas es 00C untuk menjadi es -150C
Perkembangan logika
Jadi total kalor yang harus dikeluarkan oleh lemari es untuk mengubah 10 gram air 200C menjadi es -150C adalah: